冠状病毒所致心力衰竭的组学机制分析及药物预测
冠状病毒所致心力衰竭的组学机制分析及药物预测
陈熙勐 曹丰 张皓旻 陈浩然 张钧栋 智鹏 李卓阳 王毅兴 卢学春
中华心血管病杂志, 2020,48:网络预发表. DOI: 10.3760/cma.j.cn112148-20200308-00172
摘要
目的 探讨冠状病毒感染所致心力衰竭(心衰)的机制,并预测对其可能有疗效的药物。
方法 在基因表达数据库(GEO)检索冠状病毒和心衰,并筛选符合实验要求的组学数据。采用R语言Limma程序包进行差异表达基因分析,筛选差异表达基因。将两组差异基因导入R语言clusterProfiler包进行基因本体学(GO)和京都基因与基因组百科全书(KEGG)通路富集分析,取两组结果的交集。采用STRING数据库对所有差异表达基因构建蛋白质互作网络并筛选核心基因。最后采用团队自主研发的表观精准治疗预测平台EpiMed预测冠状病毒所致心衰的治疗药物。
结果 在GEO数据库检索并筛选得到GSE59185冠状病毒数据集,根据不同的亚型分为wt组、∆E组、∆3组、∆5组、对照组5组样本,差异分析发现各亚组交集上调基因191个,下调基因18个。在GEO数据库检索并筛选得到GSE126062心衰数据集,共筛选差异表达基因495个,其中上调165个,下调330个。冠状病毒与心衰差异表达基因富集分析,取交集处理共有GO条目20条,主要富集在病毒反应、病毒防御反应、Ⅰ型干扰素反应、γ干扰素调节、先天免疫反应调节、病毒生命周期负调控、病毒基因组复制调控等;共有5条KEGG通路,主要与肿瘤坏死因子(TNF)信号通路、白细胞介素(IL)-17信号通路、细胞因子与受体相互作用、Toll样受体信号通路、人类巨细胞病毒感染有关。蛋白互作网络分析筛选出信号传导及转录激活蛋白3、IL-10、IL-17、TNF、干扰素调节因子9、2',5'-寡腺苷酸合成酶1、丝裂原活化蛋白激酶3、S-腺苷甲硫氨酸基区域蛋白2、CXC趋化因子配体10、半胱氨酸天冬氨酸蛋白酶3共10个核心基因。EpiMed平台预测可能对冠状病毒所致心衰有效的药物为TNF-α抑制剂、白藜醇、利托那韦、白芍、维甲酸、连翘、鱼腥草等。
结论 多个炎症通路的异常活化可能是冠状病毒感染所致心衰的原因,白藜芦醇、利托那韦、维甲酸、白芍、连翘、鱼腥草可能对其具有治疗作用。
冠状病毒是一种单链RNA病毒,主要感染鸟类和包括人在内的哺乳类动物。当前已知的可引起人类感染的冠状病毒主要有严重急性呼吸综合征冠状病毒(SARS-CoV)、中东呼吸综合征冠状病毒(MERS-CoV)以及2019新型冠状病毒(2019-nCoV)等7种,人感染后常引起咳嗽、发热、呼吸困难等症状[1,2],其中一些重症患者常发生心力衰竭(心衰),导致循环衰竭,危及生命。目前冠状病毒感染与心衰的关系及其机制尚不清楚,更缺乏针对性的治疗药物。早期发现并对轻、重症患者进行有效的心肌细胞保护对于减少和/或避免患者向重症、危重症进展具有重大意义。本研究通过生物信息学方法,探究了冠状病毒感染与心衰的关系及其机制,探究了潜在的治疗药物,以期为临床治疗提供理论依据。
本研究数据来源于基因表达数据库(GEO),该数据库由美国国立生物信息中心创建并维护,收录了世界各国研究机构提交的高通量基因表达数据。本研究分别以"coronavirus"和"heart failure"关键词在GEO数据库中进行检索,以全基因组表达芯片数据或转录组测序数据、有对照组、每组至少3个生物学重复以及实验设计思路清晰为标准筛选数据。
对下载数据表达值与基因注释信息匹配,如多个探针对应一个基因,则采用所有探针表达值的平均值作为此基因的表达值,利用Bioconductor中的Impute程序包补全缺失值,形成基因表达矩阵。若数据来源物种为小鼠或大鼠,则采用R语言biomaR程序包将基因名对应至人源基因。全基因组表达芯片数据采用R程序语言Limma程序包以|logFC|>1,FDR<0.05为阈值筛选差异表达基因,logFC>1定义为上调基因,logFC<-1定义为下调基因。
采用R语言clusterProfiler包进行基因本体学(GO)和京都基因与基因组百科全书(KEGG)通路富集分析。将差异表达基因导入R语言程序,以FDR<0.05,P<0.05作为筛选阈值,得到富集的GO和KEGG通路。将冠状病毒与心衰差异基因分别进行GO和KEGG富集分析,取交集作为后续分析对象。
将冠状病毒和心衰差异表达基因合并去重后,上传至STRING数据库构建蛋白质互作(protein-protein interaction,PPI)网络。以可靠性阈值>0.9作为截断值并将数据下载。随后将数据导入Cytoscape可视化分析软件对PPI网络进行可视化分析,使用Cytohubba插件评估网络中基因节点的重要性,选取该插件网络中心性节点排名前10位的基因作为核心基因。
本研究团队前期基于"系统生物学"和"比较功能基因组学"理论设计了"整合多组学分析"算法,并以此为基础建立了涵盖所有疾病、中药、化合物的人体功能基因组学数据的表观精准治疗预测平台(Epigenomic Precision Medicine Prediction Platform,EpiMed)。应用该平台对冠状病毒和心衰差异表达基因进行多组学关联分析,以关联强度<0.1、P<0.05的药物为可能具有疗效的药物。
以"coronavirus"在GEO数据库中检索,共检索到1 955个数据集,按筛选标准最终确定冠状病毒数据采用GSE59185数据集。该数据集基于GPL13912平台,采用Agilent-028005 SurePrint G3 Mouse GE 8x60K微阵列芯片检测了15只Balb/c小鼠的肺组织样本。根据病毒亚型分为rSARS-CoV-MA15-wt组(wt组)、rSARS-CoV-MA15-∆E组(∆E组)、rSARS-CoV-MA15-∆3组(∆3组)、rSARS-CoV-MA15-∆5组(∆5组)、Mock组(对照组)5组样本,每组3个生物学重复样本。将wt组、∆E组、∆3组、∆5组与对照组分别进行差异表达基因分析。以"heart failure"在GEO数据库检索,共检索到2 761个数据集,根据筛选标准最终确定心衰数据采用GSE126062数据集。该数据集基于GPL14746平台,采用Agilent-028282 Whole Rat Genome Microarray 4x44K v3微阵列芯片检测了6只大鼠心脏组织样本,包括心衰组和健康对照组2组样本,每组3个生物学重复样本。将心衰组与健康对照组进行差异表达基因分析。
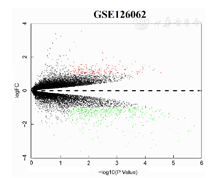
按照筛选阈值,冠状病毒数据中,wt组共筛选差异表达基因1 544个,其中上调基因789个,下调基因755个;∆E组共筛选差异表达基因469个,其中上调基因278个,下调基因191个;∆3组共筛选差异表达基因857个,其中上调基因573个,下调基因284个;∆5组共筛选差异表达基因736个,其中上调基因508个,下调基因228个。对各组上调基因和上调基因分别取交集后,发现共同差异基因209个,其中上调基因191个,下调基因18个(图1)。心衰数据中,共筛选差异表达基因495个,其中上调165个,下调330个(图2)。
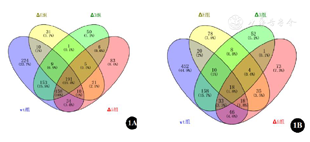
冠状病毒差异基因共富集407条GO条目,13条KEGG通路。心衰差异基因共富集93条GO条目,7条KEGG通路。经取交集处理,共有GO条目20条,主要富集在病毒反应、病毒防御反应、Ⅰ型干扰素反应、γ干扰素调节、先天免疫反应调节、病毒生命周期负调控、病毒基因组复制调控等;共有5条KEGG通路,主要与肿瘤坏死因子(TNF)信号通路、白细胞介素(IL)-17信号通路、细胞因子与受体相互作用、Toll样受体信号通路、人类巨细胞病毒感染有关。
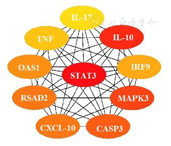
冠状病毒和心衰的蛋白互作网络分析共得到1 620个蛋白,4 703条相互关系。冠状病毒和心衰差异基因筛选得到排名前10位的核心基因为信号传导及转录激活蛋白3(STAT3)、IL-10、IL-17、TNF、干扰素调节因子9、2',5'-寡腺苷酸合成酶、丝裂原活化蛋白激酶3(MAPK3)、S-腺苷甲硫氨酸基区域蛋白2、CXC趋化因子配体10(CXCL-10)、半胱氨酸天冬氨酸蛋白酶(CASP3)(图3)。

EpiMed平台预测可能对冠状病毒所致心衰有效的药物多与抗病毒药物、血管活性药物、免疫调节剂等有关,包括TNF-α抑制剂、白藜醇、利托那韦、白芍、维甲酸、连翘、鱼腥草等。
冠状病毒是广泛存在于自然界中的一大类病毒,冠状病毒感染常导致肠道或呼吸系统疾病,但研究发现在严重急性呼吸综合征(SARS)和新型冠状病毒肺炎(COVID-19)的部分患者中均观察到了心肌损伤,而其中一部分患者会发生心衰,危及生命[3,4]。目前关于2019-nCoV引起心衰的机制尚不明确,亦缺乏针对性治疗措施,一旦暴发将导致患者病情急剧恶化甚至死亡。本研究通过生物信息学分析,筛选出冠状病毒感染与心衰的共同通路及调控基因,并采用EpiMed表观精准治疗预测平台对相关药物进行了预测,以期为临床治疗提供理论依据。
冠状病毒感染细胞以后,会引起多种分子、信号通路、转录调控等全基因组范围的变化。本研究发现,冠状病毒与心衰的差异基因均富集于TNF信号通路、IL-17信号通路、细胞因子与受体相互作用、Toll样受体信号通路等,PPI网络中的核心基因STAT3、IL-10、IL-17、TNF-α、MAPK3等多与免疫分子相关。值得注意的是,TNF信号通路中富集了大量冠状病毒与心衰共同的差异基因,如TNFR2、RIP1、PI3K、TNF、CCL2、CASP3等。研究表明,人感染SARS-CoV后,机体免疫系统被充分激活,IL-2、IL-4、IL-6、IL-10、TNF-α等指标均高于正常水平[5]。Huang等[3]发现,2019-nCoV感染患者IL-1β、干扰素-γ、干扰素诱导蛋白-10等促炎因子升高。在COVID-19重症患者血清中的IL-2、IL-7、IL-10、TNF-α浓度亦高于轻症患者,表现出全身过度炎症反应,诱发细胞因子风暴[6]。通过COVID-19患者尸检发现,患者双肺出现弥漫性肺泡损伤伴纤维黏液样渗出物,大量细胞脱落和透明膜形成,肺泡间质内出现以淋巴细胞为主的单核细胞炎性浸润[9]。因此,我们推测人感染冠状病毒后激活了凋亡信号通路,由于细胞免疫的持续激活介导,过度免疫反应打开了炎症网络中炎症级联的"金字塔顶",由此引发的细胞因子风暴可能是心肌损伤的重要机制,而左心室扩张和重塑最终导致了心脏收缩功能障碍和心衰[7,8]。
针对以上信号通路的改变,本研究采用团队自主研发的EpiMed表观精准治疗预测平台对疾病-药物进行关联分析,结果显示TNF-α抑制剂、白藜芦醇、维甲酸、鱼腥草、连翘等可能具有治疗冠状病毒感染及其所致心衰的作用。有关心衰发病机制的研究发现,TNF可导致心肌收缩功能障碍,引起心肌肥厚,并诱导心肌细胞凋亡,推测抑制该细胞因子可能会使心衰患者获益。Listing等[10]发现,TNF-α抑制剂对心衰有保护因素。还有研究发现,TNF-α抑制剂英夫利昔单抗治疗可改善患者心功能、降低心衰生物标志物水平[11]。本研究预测的可能对冠状病毒所致心衰具有治疗效果的药物,如白藜芦醇、维甲酸、鱼腥草等中草药,既往研究显示他们具有控制患者血清IL-8、TNF-α及IL-1β数量,调节TNF-α、IL-6等促炎因子水平,从而减轻炎症反应的作用[12,13,14,15,16]。因此,我们推测这些药物可能通过抑制过度免疫反应缓解冠状病毒引起的肺部炎症,降低过度炎症反应引发心衰的风险。
本研究的不足之处在于未能通过细胞实验进一步验证和直接获取2019-nCoV感染开源数据。未来,随着细胞实验和临床实践的验证以及冠状病毒感染相关组学数据的不断积累,有望进一步明确冠状病毒感染引发心衰的机制及其针对性药物。
综上所述,多个炎症通路的异常活化可能是冠状病毒感染引发心衰的原因,TNF-α抑制剂、白藜芦醇、利托那韦、维甲酸、连翘、鱼腥草可能对其具有治疗作用。
利益冲突 所有作者均声明不存在利益冲突
[16]许贵军,李志军,王琦,等.鱼腥草的抗炎活性成分[J].中国药科大学学报,2016,47(3):294-298. DOI: 10.11665/j.issn.1000-5048.20160308.
来源:中华心血管病杂志